André Julião | Agência FAPESP – Estudo publicado na revista Science Advances sugere que um tipo de tratamento conhecido como inibidor de checkpoint imunológico – já usado contra certos tipos de câncer – pode ser benéfico em alguns casos graves de COVID-19. Os criadores desse tipo de terapia, que tem a capacidade de reativar o sistema imune, ganharam o Prêmio Nobel de Medicina em 2018.
As conclusões do artigo se baseiam em experimentos feitos com células de pacientes que precisaram ser internados em Unidade de Terapia Intensiva (UTI) após contrair o SARS-CoV-2, além de camundongos infectados por outro betacoronavírus, o MHV-A59 (vírus da hepatite murina A59).
“Um dos checkpoints imunológicos conhecidos e com o qual trabalhamos no estudo é o PD-1. Ele indica para os linfócitos T [um tipo de leucócito] que devem parar de responder à infecção depois de um tempo, para que não haja uma resposta exacerbada. Num contexto de câncer, sepse ou COVID-19 grave, porém, o PD-1 faz com que os linfócitos T parem de funcionar antes mesmo de resolvida a doença. Por isso, é preciso bloqueá-lo”, explica Pedro Moraes-Vieira, professor do Instituto de Biologia da Universidade Estadual de Campinas (IB-Unicamp) apoiado pela FAPESP e um dos coordenadores do estudo.
O trabalho tem como um dos autores Gustavo Gastão Davanzo, doutorando no IB-Unicamp e bolsista da FAPESP.
“Ainda que estes sejam tratamentos de custo muito elevado, o fato de não haver mais tantos pacientes graves como no começo da pandemia nos faz acreditar que esta seria uma das opções viáveis, caso novos estudos mostrem que a terapia é segura em pacientes com COVID-19”, afirma Moraes-Vieira.
Coronavírus de camundongo
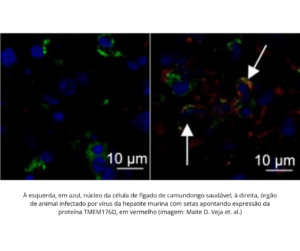
A hipótese do estudo surgiu quando pesquisadores uruguaios – coautores do artigo – observaram que camundongos que não expressavam a proteína TMEM176D tinham respostas mais agudas à infecção pelo MHV-A59. Essa proteína tem como função regular o chamado inflamassoma, complexo proteico existente dentro das células de defesa que controla a inflamação em um organismo com o objetivo de destruir ameaças como tumores, vírus e bactérias.
Sem a proteína TMEM176D, o inflamassoma fica ainda mais ativado, com maior liberação de citocinas inflamatórias, como a interleucina-1 beta (IL-1β), cujo papel é conhecido na COVID-19 grave (leia mais em: agencia.fapesp.br/34680/).
“Essa liberação excessiva de IL-1β leva a uma disfunção dos linfócitos T, o que chamamos de exaustão dessas células de defesa. Elas ficam tão ativadas que não conseguem mais responder adequadamente. É algo bem comum em doenças virais crônicas, como a COVID-19 grave, algo que já tínhamos observado em um trabalho ainda no começo da pandemia”, conta Moraes-Vieira.
O trabalho a que o pesquisador se refere foi publicado em 2020 na Cell Metabolism e ainda hoje está entre os artigos mais citados da revista nos últimos três anos, tendo motivado o contato da equipe uruguaia para propor a parceria (leia mais em: agencia.fapesp.br/33237/).
Nos testes com camundongos, o tratamento com inibidor de PD-1 conseguiu restaurar a função dos linfócitos T. Além disso, os pesquisadores tiveram acesso a sangue de doadores saudáveis e de pacientes com COVID-19 internados em duas instituições de Montevidéu, no Uruguai.
Experimentos com células saudáveis, posteriormente infectadas com o SARS-CoV-2, foram realizados no Laboratório de Estudos de Vírus Emergentes (LEVE) sob coordenação de José Luiz Proença Módena, professor do IB-Unicamp apoiado pela FAPESP e coautor do artigo.
Nos testes com amostras de pacientes, apenas as células que vieram de internados em UTI tiveram benefício com a administração do atezolizumab, droga inibidora do PD-1 usada no estudo. Isso ocorre justamente porque são esses pacientes que têm ativação exacerbada do inflamassoma, o que leva a esse perfil de exaustão e disfunção da imunidade adaptativa.
Os pesquisadores alertam que os resultados ainda precisam ser vistos com cautela. Estudos com pacientes de câncer que já faziam uso da terapia antes de contraírem a COVID-19 não mostraram benefício ou mesmo resultaram em uma associação negativa.
Em um deles, a administração da terapia antes da infecção viral não levou à melhora do quadro de COVID-19. Em outro trabalho, que acompanhou 423 pacientes, houve mais casos de hospitalização e severidade da doença entre aqueles que haviam recebido o inibidor. Por outro lado, um estudo clínico com inibidores de PD-1 em pacientes com sepse mostrou que a terapia é segura. Novos estudos, portanto, serão necessários para conhecer melhor os efeitos do tratamento no contexto da COVID-19.
O artigo PD-1/PD-L1 blockade abrogates a dysfunctional innate-adaptive immune axis in critical β-coronavirus disease pode ser lido em: www.science.org/doi/10.1126/sciadv.abn6545.


