Luciana Constantino | Agência FAPESP – Uma terapia celular inovadora, que vem sendo utilizada para tratamento de câncer, mostrou-se promissora no controle de infecções causadas por fungos. Estudo publicado na revista científica Cytotherapy apontou que o uso de células CAR-T (sigla em inglês para receptor de antígeno quimérico) programadas para “reconhecer” fungos Cryptococcus spp. foi eficiente no controle da propagação desses microrganismos in vitro e em camundongos.
O Cryptococcus gattii e Cryptococcus neoformans – presentes em solo com matéria orgânica morta e encontrados em locais contaminados com fezes de pássaros, principalmente pombos – provocam micose sistêmica no organismo humano. Podem afetar o pulmão e o sistema nervoso central. Por isso, os sintomas variam de acordo com o local em que se alojaram, podendo provocar desde uma infecção pulmonar até uma meningite ou meningoencefalite. A transmissão ocorre por meio da inalação dos fungos. Dependendo da gravidade, leva à morte.
A cada ano, cerca de 1 milhão de casos de infecção por Cryptococcus são registrados em todo o mundo, de acordo com dados do Centro de Controle e Prevenção de Doenças (CDC, em inglês). A taxa de mortalidade varia entre 20% e 70%. Ainda segundo a agência do Departamento de Saúde dos Estados Unidos, são notificados 220 mil casos de meningite criptocócica anualmente, afetando principalmente pacientes com Aids, doença causada pelo HIV.
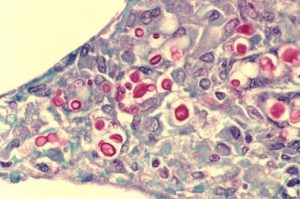
Uso de células CAR-T programadas para “reconhecer” Cryptococcus spp. foi eficiente no controle da propagação in vitro e em camundongos (criptococose pulmonar; imagem: Wikimedia Commons)
Para escapar do sistema de defesa do hospedeiro, o Cryptococcus se reveste de uma cápsula à base de carboidratos (polissacarídeos), composta majoritariamente de glucuronoxilomanana (GXM), considerada o principal fator de virulência do fungo. No organismo humano, as células de defesa T CD4+ e T CD8+ têm dificuldade de reconhecer o Cryptococcus e de combater sua proliferação.
No estudo Glucuronoxylomannan in the Cryptococcus species capsule as a target for Chimeric Antigen Receptor T-cell therapy, cujo primeiro autor é o pesquisador brasileiro Thiago Aparecido da Silva, da Faculdade de Medicina de Ribeirão Preto, da Universidade de São Paulo (USP), o grupo desenhou um CAR direcionado à GXM, com o objetivo de fazer com que as células reconhecessem diretamente o fungo e atuassem para conter seu crescimento.
“Esses achados revelam que as células GXMR-CAR-T são redirecionadas para reconhecer o Cryptococcus neoformans. Estudos futuros serão focados na determinação dos mecanismos envolvidos na eficácia terapêutica dessas células em um modelo animal de criptococose [como é chamada a infecção]”, concluem os pesquisadores no artigo.
Segundo Silva, além de conter o crescimento do fungo, a infusão de células GXMR-CAR-T também reduziu as chamadas células gigantes – leveduras com diâmetro maior (acima de 45 micrômetros) presentes durante a infecção por Cryptococcus e que aumentam sua virulência. Silva é pesquisador do Departamento de Biologia Celular, Molecular e Bioagentes Patogênicos (Biocel), da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (FMRP-USP), e tem apoio da FAPESP por meio de Bolsa de Pós-Doutorado e de uma Bolsa Estágio de Pesquisa no Exterior (BEPE).
“Essa redução das leveduras gigantes indica um bom prognóstico para novos tratamentos para criptococose. Células CAR-T podem ser utilizadas para outras infecções fúngicas e associadas a uma terapia tradicional, diminuindo assim os atuais efeitos colaterais desses medicamentos. Com células CAR-T é possível estabelecer uma memória imunológica para o paciente frente a infecções fúngicas invasivas, podendo atuar como um protetor em casos de reinfecção”, explica o pesquisador, em entrevista à Agência FAPESP.
Agora, apoiado pela FAPESP por meio de um Auxílio à Pesquisa na modalidade Jovem Pesquisador, ele está buscando otimizar a resposta protetora das células CAR-T, com foco também nos fungos Candida albicans e Histoplasma capsulatum.
Morte direta de fungos
O grupo de pesquisadores do MD Anderson Cancer Center, no Texas, Estados Unidos, colaborador de Silva, foi o primeiro a explorar a morte direta de fungos com o redirecionamento de células T CD8+ por meio de um receptor de antígeno quimérico (CAR) projetado para atingir um carboidrato encontrado na parede celular do fungo Aspergillus fumigatus.
O interesse no uso de células CAR-T para tratamento de doenças como o câncer vem aumentando nos últimos anos em vários países. Na maioria dos estudos com essa técnica, os pesquisadores utilizaram o receptor de CD19 como alvo para conter a multiplicação anormal (neoplasia) de células B, que podem ocasionar consequências graves ao organismo (leia mais em: agencia.fapesp.br/31656/).
Desde 2017, a agência americana Food and Drug Administration vem dando aval à aplicação de terapias de células CAR-T, principalmente no tratamento de leucemia e de linfoma.
No Brasil, outro grupo de pesquisadores do Centro de Terapia Celular (CTC) da USP em Ribeirão Preto, um Centro de Pesquisa, Inovação e Difusão (CEPID) apoiado pela FAPESP, testou pela primeira vez, em 2019, o uso desse tratamento inovador contra o câncer, feito com células reprogramadas do próprio paciente.
A técnica foi usada para tratar um caso avançado de linfoma difuso de células B – um tipo de linfoma não Hodgkin, doença que afeta o sistema linfático (leia mais em agencia.fapesp.br/31656/). Em fevereiro de 2020, o CDC lançou um livro reunindo informações práticas para orientar a produção de células CAR-T (saiba mais em agencia.fapesp.br/32526/).
Reconhecimento do alvo
No caso da pesquisa desenvolvida pelo grupo do qual Silva faz parte, os autores levantaram a hipótese de que as células GXMR-CAR-T apresentariam atividade citotóxica contra fungos que expressam a glucuronoxilomanana na parede celular. O estudo demonstrou que células T humanas modificadas expressando GXMR-CAR se ligaram ao carboidrato GXM em solução e interagiram com levedura de Cryptococcus neoformans.
“O mais crítico na construção de um CAR é a porção de reconhecimento do alvo, em que utilizamos anticorpos monoclonais que interagem com o Cryptococcus. Usamos a sequência de DNA que codifica a porção do anticorpo que reconhece o fungo e colocamos em conjunto com a sequência de DNA codificadora das outras porções do CAR”, explica Silva.
Leia o artigo Glucuronoxylomannan in the Cryptococcus species capsule as a target for Chimeric Antigen Receptor T-cell therapy em www.isct-cytotherapy.org/article/S1465-3249(20)30933-6/fulltext.


